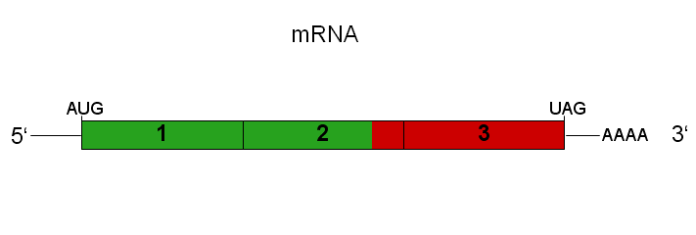
Toisin kuin tavanomainen mRNA rokotteet joka koodaa vain kohdeantigeenejä, itse monistuvat mRNA:t (saRNA:t) koodaa myös ei-rakenneproteiineja ja promoottoria, mikä tekee saRNA:t replikonit, jotka pystyvät transkriptoimaan in vivo isäntäsoluissa. Varhaiset tulokset osoittavat, että niiden tehokkuus pienempinä annoksina on sama kuin tavanomaisten annosten teho. mRNA. Pienten annosvaatimusten, harvempien sivuvaikutusten ja pidemmän vaikutuksen keston vuoksi saRNA näyttää paremmalta RNA-alustalta rokotteille (mukaan lukien mRNA COVID -rokotteiden v.2.0) ja uudemmille hoitoaineille. Mitään saRNA-pohjaista rokotetta tai lääkettä ei ole vielä hyväksytty ihmiskäyttöön. Merkittävä edistys tällä alalla voi kuitenkin käynnistää infektioiden ja rappeuttavien sairauksien ehkäisyn ja hoidon renessanssin.
Tarpeetonta sanoa, että ihmiskunta on hauras ennen COVIDin kaltaisia pandemioita. Me kaikki koimme sen ja vaikutimme meihin tavalla tai toisella; miljoonat eivät voineet nähdä seuraavana aamuna. Koska Kiinallakin oli massiivinen COVID-19-rokotusohjelma, viimeisimmät tiedotusvälineiden tapaukset ja kuolleisuus Pekingissä ja sen ympäristössä ovat huolestuttavia. Tarvitaan valmistautumista ja säälimätöntä tehokkaampaa rokotteet ja terapiaa ei voi vähätellä.
COVID-19-pandemian tarjoama poikkeuksellinen tilanne tarjosi tilaisuuden lupaavalle RNA teknologia päästä eroon iästä. Kliiniset tutkimukset voitaisiin saattaa päätökseen ennätysvauhtia ja mRNA perustuu COVID rokotteet, BNT162b2 (valmistaja Pfizer/BioNTech) ja mRNA-1273 (Moderna) sai EUA:n sääntelijöiltä ja sillä oli aikanaan tärkeä rooli pandemiaa vastaan kansoille erityisesti Euroopassa ja Pohjois-Amerikassa1. Nämä mRNA rokotteet perustuvat synteettisiin RNA-alustoille. Tämä mahdollistaa nopean, skaalautuvan ja soluttoman teollisen tuotannon. Mutta nämä eivät ole ilman rajoituksia, kuten korkeat kustannukset, kylmä toimitusketju, pienenevät vasta-ainetiitterit, muutamia mainitakseni.
mRNA rokotteet tällä hetkellä käytössä (kutsutaan joskus tavanomaiseksi tai 1. sukupolveksi mRNA rokotteet) perustuvat virusantigeenin koodaamiseen synteettisessä RNA:ssa. Ei-viraalinen kuljetusjärjestelmä kuljettaa transkriptin isäntäsolun sytoplasmaan, jossa virusantigeeni ekspressoituu. Ilmentynyt antigeeni indusoi sitten immuunivasteen ja aikaansaa aktiivisen immuniteetin. Koska RNA hajoaa helposti ja tämä rokotteessa oleva mRNA ei pysty transkriptoimaan itseään, huomattava määrä synteettisiä virus-RNA-transkriptejä (mRNA) on annettava rokotteessa halutun immuunivasteen aikaansaamiseksi. Mutta entä jos synteettinen RNA-transkripti liitetään halutun virusantigeenin lisäksi myös ei-rakenteellisiin proteiineihin ja promoottorigeeneihin? Sellainen RNA transkriptilla on kyky transkriptoida tai vahvistaa itseään, kun se kuljetetaan isäntäsoluun, vaikka se on pidempi ja raskaampi ja sen kuljetus isäntäsoluihin voi olla monimutkaisempaa.
Toisin kuin perinteiset (tai ei-vahvistavat) mRNA jolla on koodit vain kohdistetulle virusantigeenille, itseään vahvistavalle mRNA (saRNA) kykenee transkriptoimaan itsensä in vivo isäntäsoluissa vaadittujen ei-rakenneproteiinien koodien ja promoottorin läsnäolon ansiosta. Itsemonistuviin mRNA:ihin perustuvia mRNA-rokoteehdokkaita kutsutaan toiseksi tai seuraavaksi sukupolveksi mRNA rokotteet. Ne tarjoavat parempia mahdollisuuksia pienempien annosvaatimusten, suhteellisen harvempien sivuvaikutusten ja pidemmän vaikutuksen/vaikutusten keston suhteen. (2-5). Molemmat RNA-alustan versiot ovat tiedeyhteisön tiedossa jo jonkin aikaa. Pandemiareaktiossa tutkijat valitsivat rokotteiden kehittämiseen replikoitumattoman version mRNA-alustan yksinkertaisuuden ja pandemiatilanteen välttämättömyyden vuoksi ja hankkivat ensin kokemusta monistamattomasta versiosta, jos varovaisuus on perusteltua. Nyt meillä on kaksi hyväksyttyä mRNA:ta rokotteet COVID-19:ää vastaan ja useita valmisteilla olevia rokote- ja terapeuttisia aineita, kuten HIV-rokote ja - hoito Charcot-Marie-Toothin tauti.
saRNA-rokoteehdokkaat COVID-19:ää vastaan
Kiinnostus saRNA-rokotteita kohtaan ei ole kovin uutta. Muutaman kuukauden sisällä pandemian alkamisesta, vuoden 2020 puolivälissä, McKay et ai. oli esittänyt saRNA-pohjaisen rokoteehdokkaan, jolla oli korkeat vasta-ainetiitterit hiiren seerumeissa ja hyvä viruksen neutralointi6. Vaiheen 1 kliininen tutkimus VLPCOV-01:stä (itsestään vahvistuva RNA rokoteehdokas) 92 terveellä aikuisella, joiden tulokset julkaistiin preprintissä viime kuussa, päättelivät, että tämän pienen annoksen antaminen saRNA perustuva rokoteehdokas indusoi immuunivaste, joka on verrattavissa tavanomaiseen mRNA-rokotteeseen BNT162b2 ja suosittelee sen jatkokehitystä tehosterokotteena7. Toisessa äskettäin julkaistussa tutkimuksessa, joka tehtiin osana COVAC1-kliinistä tutkimusta tehosteannoksen antostrategian kehittämiseksi, ylivoimainen immuunivaste havaittiin ihmisillä, joilla oli aiemmin COVID-19 ja jotka saivat uuden itseään vahvistavan lääkkeen. RNA (saRNA) COVID-19-rokote sekä Isossa-Britanniassa hyväksytty rokote8. Prekliininen tutkimus uudesta oraalista rokoteehdokkaista, joka perustuu itsevahvistukseen RNA hiirimallissa sai aikaan korkean vasta-ainetiitterin9.
saRNA-rokoteehdokas influenssaa vastaan
Influenssa rokotteet Tällä hetkellä käytössä olevat tuotteet perustuvat inaktivoituihin viruksiin tai synteettisiin rekombinantteihin (synteettinen HA-geeni yhdistettynä bakulovirukseen)10. Itseään vahvistava mRNA-pohjainen rokoteehdokas voi indusoida immuniteetin useita virusantigeenejä vastaan. Prekliininen tutkimus sa-mRNA-biskistronic A/H5N1 -rokoteehdokkaista influenssaa vastaan hiirillä ja freteillä sai aikaan voimakkaita vasta-aineita ja T-soluvasteita, jotka oikeuttavat arvioinnin ihmisillä kliinisissä tutkimuksissa11.
COVID-19-rokotteet ovat saaneet huomiota ilmeisistä syistä. Joitakin esikliinisiä töitä RNA-alustojen soveltamiseksi on tehty muiden infektioiden ja ei-infektiivisten sairauksien, kuten syöpien, Alzheimerin taudin ja perinnöllisten sairauksien, varalta; mitään saRNA-pohjaista rokotetta tai lääkettä ei kuitenkaan ole vielä hyväksytty ihmiskäyttöön. SaRNA-pohjaisten rokotteiden käyttöä on tutkittava lisää, jotta voidaan ymmärtää kokonaisvaltaisesti niiden turvallisuus ja tehokkuus ihmisillä käytettäessä.
***
Viitteet:
- Prasad U., 2020. COVID-19 mRNA-rokote: Tieteen virstanpylväs ja lääketieteen pelin muuttaja. Tieteellinen eurooppalainen. Julkaistu 29. joulukuuta 2020. Saatavilla verkossa osoitteessa http://scientificeuropean.co.uk/medicine/covid-19-mrna-vaccine-a-milestone-in-science-and-a-game-changer-in-medicine/
- Bloom, K., van den Berg, F. & Arbuthnot, P. Itsevahvistuvat RNA-rokotteet infektiosairauksia varten. Gene Ther 28, 117 - 129 (2021). https://doi.org/10.1038/s41434-020-00204-y
- Pourseif MM et ai 2022. Itsevahvistuvat mRNA-rokotteet: Toimintatapa, suunnittelu, kehitys ja optimointi. Huumeiden löytö tänään. Osa 27, numero 11, marraskuu 2022, 103341. DOI: https://doi.org/10.1016/j.drudis.2022.103341
- Blakney AK et ai 2021. Päivitys itseään vahvistavasta mRNA-rokotteen kehittämisestä. Rokotteet 2021, 9(2), 97; https://doi.org/10.3390/vaccines9020097
- Anna Blakney; Seuraavan sukupolven RNA-rokotteet: itsestään monistuva RNA. Biochem (Lontoo) 13. elokuuta 2021; 43 (4): 14–17. doi: https://doi.org/10.1042/bio_2021_142
- McKay, PF, Hu, K., Blakney, AK et ai. Itsestään monistuva RNA SARS-CoV-2 -lipidinanohiukkasrokoteehdokas indusoi korkeat neutraloivat vasta-ainetiitterit hiirissä. Nat Commun 11, 3523 (2020). https://doi.org/10.1038/s41467-020-17409-9
- Akahata W., et al 2022. SARS-CoV-2-itsevahvistuvan RNA-rokotteen turvallisuus ja immunogeenisyys, joka ilmentää ankkuroitua RBD:tä: satunnaistettu, tarkkailijasokea, vaiheen 1 tutkimus. Preprint medRxiv 2022.11.21.22281000; Julkaistu 22. marraskuuta 2022. doi: https://doi.org/10.1101/2022.11.21.22281000
- Elliott T, et ai. (2022) Tehostuneet immuunivasteet heterologisen rokotuksen jälkeen itse monistuvilla RNA- ja mRNA-COVID-19-rokotteilla. PLoS Pathog 18(10): e1010885. Julkaistu: 4. lokakuuta 2022. DOI: https://doi.org/10.1371/journal.ppat.1010885
- Keikha, R., Hashemi-Shahri, SM & Jebali, A. Uusien suun kautta otettavien rokotteiden arviointi, jotka perustuvat itsevahvistuviin RNA-lipidinanpartikkeleihin (saRNA LNP:ihin), saRNA-transfektoituihin Lactobacillus plantarum LNP:ihin ja saRNA-transfektoituihin Lactobacillus plantarum SARS-CoV:n neutraloimiseksi -2 varianttia alfa ja delta. Sci Rep 11, 21308 (2021). Julkaistu: 29. https://doi.org/10.1038/s41598-021-00830-5
- CDC 2022. Kuinka influenssarokotteet valmistetaan. Saatavilla verkossa osoitteessa https://www.cdc.gov/flu/prevent/how-fluvaccine-made.htm saatavilla 18 joulukuussa 2022.
- Chang C., et al 2022. Itsestään monistuvat mRNA-biskitroniset influenssarokotteet nostavat ristireaktiivisia immuunivasteita hiirissä ja estävät infektioita freteillä. Molekyyliterapiamenetelmät ja kliininen kehitys. Osa 27, 8. joulukuuta 2022, sivut 195–205. https://doi.org/10.1016/j.omtm.2022.09.013
***